Index
はじめに
データアナリティクスラボ株式会社データソリューション事業部の杉浦です。
今回、肺のCT(computed tomography)から抽出した画像特徴量を用いて、肺がんの遠隔転移予測モデルを構築しました。その中で、日常診療で広く使われる非造影CTから遠隔転移を予測すること、また、解釈性のあるモデルを構築し「肺がんの画像特徴」と「遠隔転移」との関係を調査することを目標としました。
Introduction
肺がんの遠隔転移診断について
肺がん診療では、がんの広がりの程度が治療方針や予後を大きく左右します。また診療では、腫瘍の大きさや広がり(T因子)・リンパ節転移の有無(N因子)・遠隔転移の有無(M因子)から病期を決定するTNM分類が基本となっており、これに基づいて治療方針が決められます。
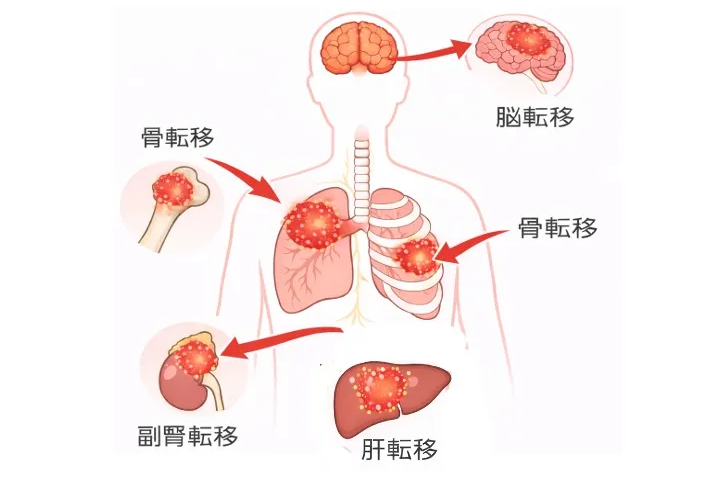
遠隔転移とは、がんが原発巣(最初にできた場所)から離れた臓器に広がった状態
画像検査は、このTNM分類を評価するための重要な手段です。一般的に、CTは原発巣のサイズや形状、広がりを評価するT因子の診断に使われます。一方、リンパ節転移や遠隔転移(N因子・M因子)の評価には、PET-CT検査(positron emission tomography)が有用とされています。また、脳転移や骨転移の評価(M因子)には、それぞれ頭部造影MRI(magnetic resonance imaging)や骨シンチグラフィが検討され、これらの検査を組み合わせて遠隔転移の有無を評価します(1)。
画像特徴量の定量化について
医用画像の定量的な特徴量としてradiomics特徴量があり、以下の種類から構成されます(2)。
- 病変の形態的特徴
- 画素値ヒストグラムの特徴量
- 画素値の空間的分布を定量化したテクスチャ特徴
視覚的に捉えやすい特徴量から人の目では観察できない高次元の特徴量まで、豊富な特徴量を定量化でき、診断や予後予測、治療効果予測への応用が進んでいます。また、日常的に取得される医用画像データを低コストで活用できる点も利点の一つです。
課題
先述の通り、肺がんの遠隔転移の評価は、造影MRIやPET-CTによる全身検索が一般的です。しかし、これらの検査には高度な設備や専門スタッフ、また高価な薬剤が必要なため、すべての施設で容易に実施できるわけではありません。一方、非造影CT(造影剤を使わないCT)は日常診療で広く行われていますが、肺がん診療では、局所病変の評価(T因子の診断)が主な役割になります。
目的
そこで本検討では、非造影CTの原発巣から抽出したradiomics特徴量を用いて、肺がんの遠隔転移予測モデルを構築します。
臨床的意義
- 非造影CTによる肺がんの遠隔転移予測は、肺がん診療を迅速に進める判断材料となる可能性があります。具体的には、PET-CTや造影MRIなどの精密検査の速やかな実施や、専門施設への適切な紹介などの判断です。
- 特に、専門の設備や人員が十分でない環境で、スタッフの意思決定支援に有用と考えます。
- また、解釈性を重視したモデル構築を行い、画像特徴量を解析することで「原発巣の画像特徴量」と「遠隔転移」の関連を考察します。
Materials & Methods
本検討では、非造影CTから腫瘍領域を抽出し、得られたマスク画像をもとにradiomics特徴量を作成・選択して予測モデルを構築しました。
1. 対象
データセットとして、The Cancer Imaging Archive の A Large-Scale CT and PET/CT Dataset for Lung Cancer Diagnosisを使いました(3)。
このデータセットには、肺がん患者のCT画像およびTNM分類等の臨床情報が収録されています。また、CT画像は、肺がんが疑われ、肺生検およびPET/CTを受けた患者から後ろ向きに取得されています。ここから、122症例を選択し治療前の非造影CTと臨床情報を用いました。Table1の使用データの臨床情報より、患者背景は特定の群に偏らない構成となっています。
遠隔転移の有無は、データセット内のTNM分類のM因子から判断し、転移あり群(n=51)および転移なし群(n=71) として定義しました。
| 項目 | 内訳 (n = 122) |
|---|---|
| 遠隔転移の有無(人) | あり:51 (41.8%) |
| 年齢(歳) | Mean ± SD : 61.1 ± 11.2 Median(IQR): 63.0(54.0 – 69.0) Range : 28 – 90 |
| 性別(人) | Female: 62 Male: 60 |
| 喫煙歴(人) | あり:42 (34.4%) |
| 装置数(台) | Biograph 64 : 10 (8.8%) Brilliance16 : 12 (10.5%) Discovery CT750 HD : 8 (7.0%) iCT 256 : 3 (2.6%) LightSpeed Pro 16 : 9 (7.9%) LightSpeed VCT : 33(28.9%) Optima CT660 : 1 (0.9%) Revolution CT : 1 (0.9%) Sensation 10 : 37 (32.5%) *8名は装置不明 |
2. 腫瘍の領域抽出
腫瘍領域の抽出には、Vision Transformerを利用した医用画像のセグメンテーションモデルMedSAM2(4)を使用しました。本モデルは Segment Anything Model 2 を医用画像向けに拡張した手法であり、1スライスに数点のプロンプトを入力し領域抽出をすると、他のスライスまで自動抽出が可能です(Fig.2)。実行は、Google Colabratory上のPython環境(GPU: NVIDIA Tesla T4)で行いました。
腫瘍の領域抽出は、専門医による手動設定が一般的ですが、大量の画像に対してスライスごとに領域を設定するため作業負荷の大きさが課題です。本検討では、MedSAM2を使うことで領域抽出の省力化を図りました。具体的には、1画像に約8スライスの腫瘍領域があったことから、1/8の作業時間短縮ができました。さらに、手作業による領域の描画を数点のプロンプト入力に代替することで、1/2以上の時間短縮ができたと考えられ、計1/16以上の時間短縮ができたと考えます。
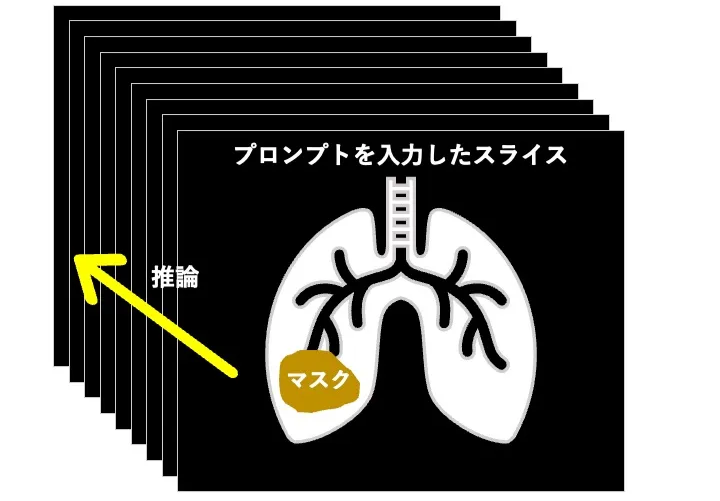
現在のスライスの画像と領域抽出で取得したマスク画像の特徴を基に、次のスライスを推論する。
領域抽出処理の流れは以下の通りです:
- CT画像をスライス単位で読み込む
- 1スライスの腫瘍領域に点プロンプトを入力
- MedSAM2を適用し、他のスライスにおいて領域抽出およびバイナリマスク生成
- 得られたマスクをradiomics特徴量の抽出に使用
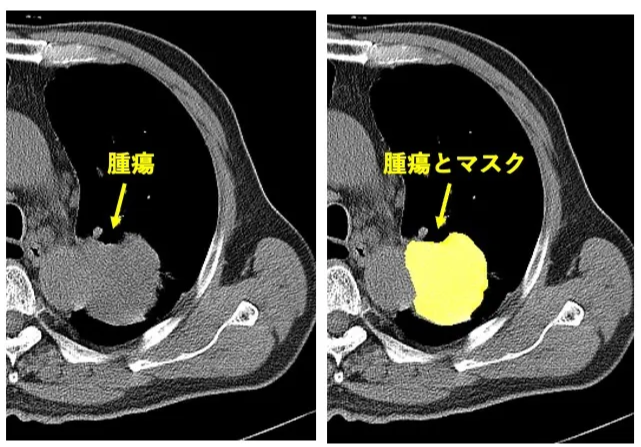
この際、階調は縦隔条件(window level=l40、window width=400)で固定し、MedSAM2による推論をしました。また、マスク画像と元画像で座標系を一致させました。
- window width:表示するCT値の幅(範囲)
- window level:CT値の範囲の中心値
- CT値:X線吸収率を数値化した物理量で、被写体組織と水のX線減弱係数をそれぞれ\(μ\)、\(μw\)として以下の式で算出される。CT画像では、CT値を画素値として扱い、空気が–1000[\(HU\)]、水が0[\(HU\)]、骨が+1000[\(HU\)]前後の値をとる。
$$ \mathrm{CT\ 値\ [HU]} = 1000 \times \frac{\mu – \mu_w}{\mu_w} $$
これらを調整することで、目的の組織や構造物を明瞭に観察します。
3. Radiomics特徴量抽出
作成したマスク画像をCT画像に適用し、腫瘍領域のradiomics特徴量を抽出しました
解析は、PythonのオープンソースパッケージであるPyRadiomics(5)を用いてスライスごと算出し、1スライス=1レコードとして保存しました。特徴量は、解釈性のよい形態的特徴量9個とヒストグラム特徴量18個を取得し、これらから特徴量選択をしました(Table 2)。
| クラス | 特徴量 | 意味 |
|---|---|---|
| 形態的特徴量 | MajorAxisLength | 関心領域を楕円近似したときの長軸の長さ |
| Elongation | 円形度、短軸÷長軸で表され、0~1の範囲で1に近いほど正円 | |
| MaximumDiameter | 最大径 | |
| MeshSurface | メッシュから算出した表面積 | |
| MinorAxisLength | 関心領域を楕円近似したときの短軸 | |
| Perimeter | 関心領域の周囲長 | |
| PerimeterSurfaceRatio | 周囲長/表面積、同じ大きさの腫瘍に対する境界の歪さを表す | |
| PixelSurface | ピクセル数×ピクセル面積、表面積 | |
| Sphericity | 円形度、1に近いほど円に近い | |
| ヒストグラム特徴量 | 10Percentile | 関心領域の画素値のうち、下位10%の値 |
| 90Percentile | 関心領域の画素値のうち、上位90%の値 | |
| Energy | 画素値の二乗和、濃度×面積を同時に見る | |
| Entropy | 画素値の分布の不規則性 | |
| InterquartileRange | 四分位範囲 | |
| Kurtosis | 分布の尖度 | |
| Maximum | 最大値 | |
| MeanAbsoluteDeviation | 平均絶対偏差 | |
| Mean | 平均値 | |
| Median | 中央値 | |
| Minimum | 最小値 | |
| Range | 最大値−最小値 | |
| RobustMeanAbsoluteDeviation | 10–90%範囲でのMAD | |
| RootMeanSquared | 二乗平均平方根 | |
| Skewness | 分布の歪み | |
| TotalEnergy | Energy×ボクセル体積 | |
| Uniformity | 一様性 | |
| Variance | 分散 |
4. モデル構築
転移予測モデルの構築にあたり、勾配ブースティング決定木アルゴリズムであるLightGBMを採用しました。
4-1. データ分割
モデルの汎化性能を評価するため、5分割交差検証を実施しました。本データセットでは、同一患者が複数のレコードを持つため、同一患者のデータが学習用と検証用データに分割されないよう、患者IDを単位とした分割を行いました。また、層化抽出により目的変数のクラス比が各分割で維持されるようにしました。
| fold | 学習データ_ 患者数 |
学習データ_ レコード数 |
テストデータ_ 患者数 |
テストデータ_ レコード数 |
学習データ_ 転移割合 |
テストデータ_ 転移割合 |
|---|---|---|---|---|---|---|
| 1 | 99 | 806 | 23 | 170 | 0.50 | 0.26 |
| 2 | 97 | 738 | 25 | 238 | 0.45 | 0.47 |
| 3 | 97 | 809 | 25 | 167 | 0.45 | 0.46 |
| 4 | 97 | 781 | 25 | 195 | 0.41 | 0.64 |
| 5 | 98 | 770 | 24 | 206 | 0.47 | 0.41 |
4-2. ハイパーパラメータ調整
ハイパーパラメータの最適化には、nested cross-validation によるランダムサーチを用いました。「決定木の数」・「学習率」・「木の深さ」・「各決定木における標本や列のサンプリング割合」を探索することで、最適なパラメータを選択しました。
4-3. 特徴量選択
モデルの過学習の抑制および汎化性向上を目的として、特徴量の選択を行いました。まず、モデルの性能をAUC(area under the curve)で評価しながら、特徴量重要度(gain)が低い特徴量を段階的に除外することで、10個まで選択しました。続けて、特徴量間の相関の強さや意味的妥当性を加味して特徴量を選択し、最終的に、Energy・MajorAxisLength・10Percentile・Range・PerimeterSurfaceRatio・Elongationの計6項目の特徴量を選択しました。
5. モデルの評価
5-1. 評価指標
性能評価では、スライス単位の予測確率を患者ごとに平均し、患者単位の予測確率および予測値を求めました。この際、感度(recall)を重視したモデルとするために、しきい値0.4以上を”転移あり”と定義しています。最終的に、5つのfoldの平均値をモデル性能としました。

性能評価には以下の指標を用いました。
- AUC
- Accuracy
- Precision
- Recall
- F1-score
5-2. 特徴量の解析
特徴量の解析には、SHAP(SHapley Additive exPlanations)を使用しました。
SAHPでは、\(X=(X1,…,XJ)\)を特徴量とした機械学習モデルを\(\hat{f}(X)\)、1つのレコードの特徴量を\(xi=(xi,1,…,xi,J)\)としたときに、あるレコードに対する予測値\(\hat{f}(xi)\)と予測の期待値\(𝔼[\hat{f}(X)]\)の差分を各特徴量の寄与度(SHAP値)に分解します。
SHAPの数式は、レコードiの特徴量\(xi\),\(j\)の貢献度(寄与度)を\(ϕi\),\(j\)として、以下の式で表されます。
$$ \hat{f}(x_i) – \mathbb{E}[\hat{f}(X)] = \sum_{j=1}^{J} \phi_{i,j} $$
Results
各評価指標の結果を以下に示します。
- AUC: 0.75 (95%CI: 0.70-0.80)
- Accuracy: 0.61 (95%CI: 0.55-0.67)
- Precision: 0.54 (95%CI: 0.45-0.63)
- Recall: 0.75 (95%CI: 0.69-0.83)
- F1-score: 0.62 (95%CI: 0.56-0.67)
最終モデルに使用した6つの特徴量を、重要度の大きい順に示します(Fig.4)。
- Energy:CT値の二乗和 [単位:HU2 × mm2]
- MajorAxisLength:関心領域を楕円近似したときの長軸の長さ [単位:mm]
- 10Percentile:関心領域の下位10%のCT値 [単位:HU]
- Range:最大CT値−最小CT値 [単位:HU]
- PerimeterSurfaceRatio:境界の歪さ [単位:/mm]
- Elongation:円形度
「長軸の長さ」と「最大CT値−最小CT値」は、予測値と正の相関が見られました (Fig.5)。
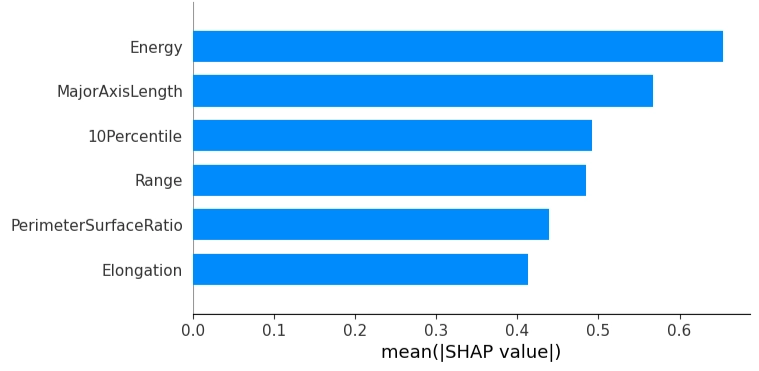
SHAP値が大きいほど、予測値への寄与度の大きい重要な特徴量と解釈できる。
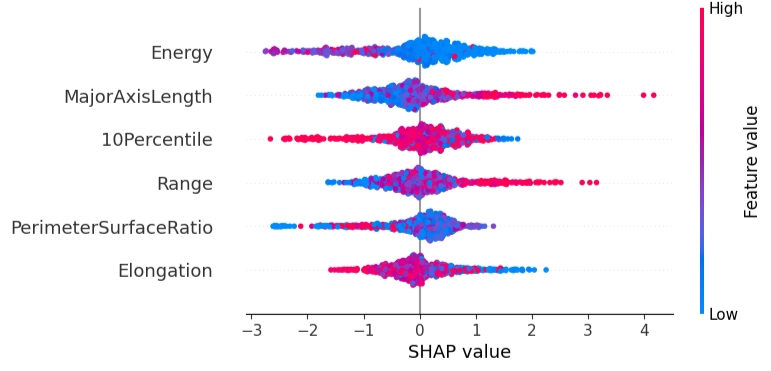
横軸がSHAP値、カラースケールが各特徴量の値の大きさを表し、色の分布とSHAP値の関係を見ることで、各特徴量と予測値の関係が分かります。例えば、赤い点が右側(正のSHAP値)に多く分布している場合、その特徴量の値が大きいほど予測値が上がること(正の相関)を意味します。
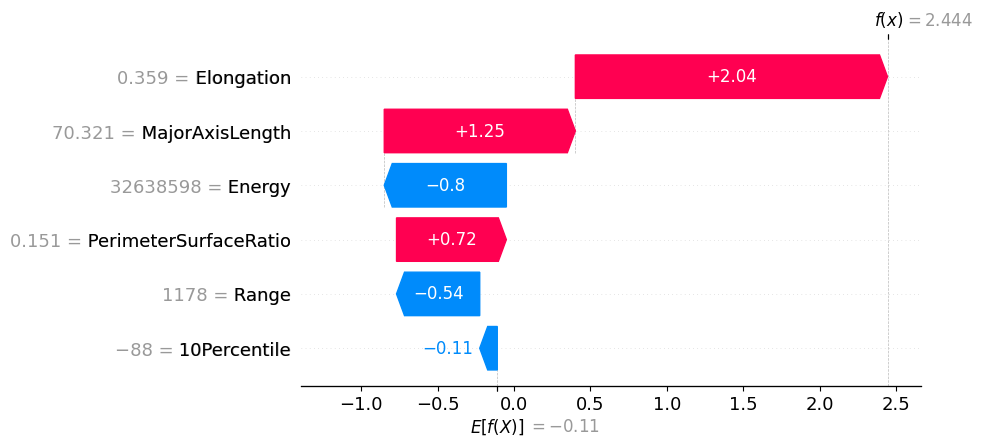
E[f(x)]が全体平均(対数オッズ)、f(x)がレコードに対する予測値。1つのレコードにおいて特徴量ごとの寄与度を評価できる。転移のある本例では、主に円形度(約0.36)と長軸の長さ(約70mm)が陽性側の予測に寄与している。
Discussion
モデルについて
肺がんの遠隔転移の診断には、専門の設備やスタッフによる精密検査が必要です。また、原発巣から直接遠隔転移を示唆する画像所見はありません。本検討では、日常診療で広く使われる非造影CTの画像特徴量を用いて肺がんの遠隔転移を予測することで、肺がん診療の意思決定支援を目指しました。本モデルの性能はAUC:0.75となり、類似研究の予測モデルのAUCが0.8前後であること(6,7)を踏まえると、改良の余地を残す結果となりました。
特徴量について
最終モデルに使用した特徴量は、以下のように視覚的な特徴と対応すると推察され、モデルに一定の解釈性を持たせることができました。
- 腫瘍の濃度:Energy
- 腫瘍のサイズ:MajorAxisLength
- 壊死やエアーの存在:10Percentile
- 内部不均一性:Range
- 辺縁の不整性:PerimeterSurfaceRatio
- 形状の歪み:Elongation
また、MajorAxisLengthとRangeは予測値と正の相関を示しました(Fig.5)。つまり、サイズが大きく、不均一であるほど遠隔転移ありと予測されます。さらに、個々のスライスの予測値と特徴量寄与度を評価し、予測根拠を理解しながら利用できることも、本モデルの有用性の1つと考えます(Fig.6)。
領域抽出について
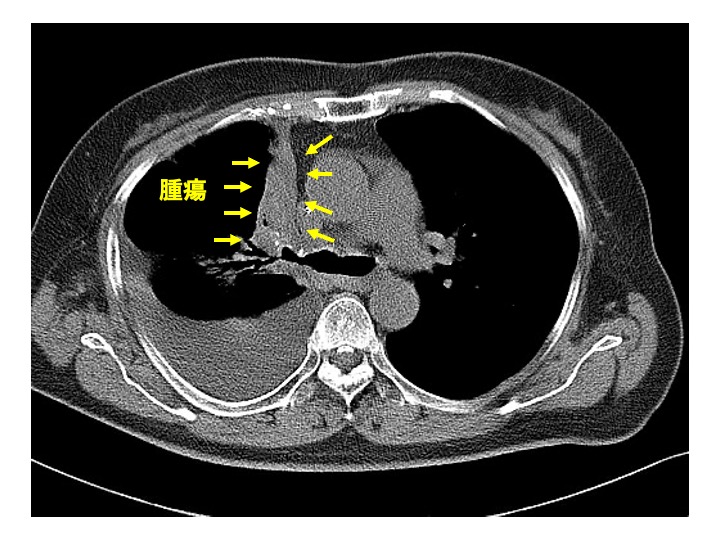
腫瘍の領域抽出は専門医による手動作成が一般的ですが、本検討では、MedSAM2を用いた半自動抽出によって行いました。これによりマスク作成を効率化できましたが、一部の症例で抽出不良を確認しました。特に、腫瘍辺縁を正確に捉えていない場合があり、形状の歪みや辺縁の不整性を表す特徴量において寄与度を下げた可能性があります(Fig.7)。このことから、今後抽出精度の向上が必要と考えます。
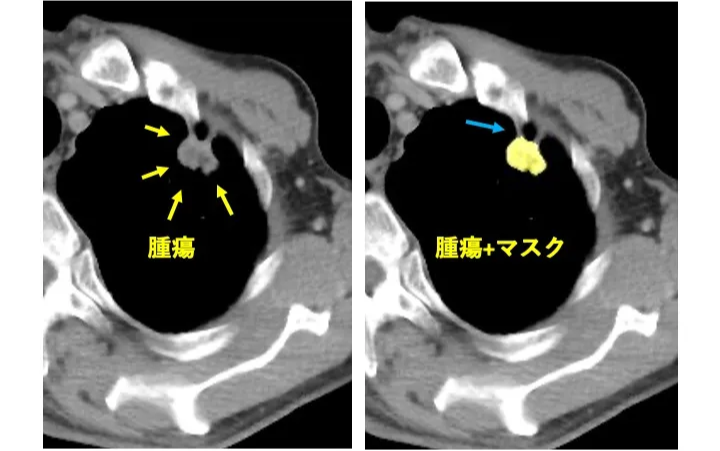
辺縁を十分に捉えきれていない部分(水色矢印)が観察できる。「転移あり」の本症例は「転移なし」と予測された。
リミテーション
本検討にはいくつか限界があります。まず、使用したデータセットの「転移あり」と「転移なし」の比率が、実際の比率と乖離している可能性があります。そのため、実際の有病率を反映した性能評価が必要と考えます。また、本検討のデータは122症例と比較的少数であり、モデルの汎用性は十分に検証されていないと言えます。今後は症例数の拡大および多施設データによる外部検証の必要性があります。
Conclusion
日常診療で広く使われる非造影CTの画像特徴量を用いて、肺がんの遠隔転移予測モデルを作成しました。モデルの性能はAUC:0.75と改善の余地はあるものの、肺がん診療を迅速に進める判断材料としての可能性を示すことができました。
References
- 画像診断ガイドライン 2021年版 p138-151
- Lambin P, et al. Radiomics: extracting more information from medical images using advanced feature analysis. Nat Rev Clin Oncol. 2012.
- Li, P., et al. A Large-Scale CT and PET/CT Dataset for Lung Cancer Diagnosis (Lung-PET-CT-Dx) [Data set]. The Cancer Imaging Archive. 2020. https://doi.org/10.7937/TCIA.2020.NNC2-0461
- Ma J, et al.MedSAM2: Segment Anything in 3D Medical Images and Videos. arXiv preprint arXiv:2504.03600. 2025.
- Van Griethuysen, et al. Computational radiomics system to decode the radiographic phenotype. Cancer research 77.21: e104-e107. 2017.
- Liu, Zheng, et al. Bone metastasis prediction in non-small-cell lung cancer: primary CT-based radiomics signature and clinical feature. BMC Medical Imaging 24.1. 2024.
- Li, Ting, et al. Application of CT radiomics in brain metastasis of lung cancer: A systematic review and meta-analysis. Clinical Imaging 114. 2024.